进行性肌营养不良(DMD/BMD)
作者:秋凉 | 发布日期:进行性肌营养不良简明指南
肌营养不良是一组肌膜结构异常导致肌肉破坏的疾病,进行性肌营养不良在这里专指由dystrophin蛋白功能障碍而导致的肌营养不良类型。根据疾病的严重程度,进行性肌营养不良被分为两种类型。杜欣氏肌营养不良(DMD)是较重的类型,而贝克型肌营养不良(BMD)是较轻的类型。进行性肌营养不良以渐进性的运动能力损害为主要临床表现。在疾病过程中,患者的小腿腓肠肌会表现出典型的假性肥大,这是DMD和BMD患者较为特征性的表现。因此,DMD和BMD也被称为假肥大型肌营养不良。进行性肌营养不良目前尚无针对性治疗方法。临床处理的主要目标是缓解病情发展、提高患者生活质量。运动康复、营养支持、体重管理与心功能保持等是最主要的对症处理方式。
编码dystrophin蛋白的DMD基因突变是造成进行性肌营养不良发生的唯一已知原因。DMD基因位于人类X染色体上,符合X连锁隐性遗传规律。男性人群中DMD患者的发病率约为1/3500,而女性携带者约为1/2300。进行性肌营养不良的发生一般遵循男性发病、女性携带的遗传特点。如果女性携带DMD基因突变,那么她生育男孩将有50%的可能成为进行性肌营养不良患者,生育女孩则有50%的可能成为DMD基因突变携带者。男性BMD患者可能生育,他所生育的男孩都是正常人,而生育的女孩则都是DMD基因突变携带者。70%-80%的进行性肌营养不良为遗传性,20%-30%的病例则来自于完全没有家族史的新发突变。
DMD基因是进行性肌营养不良的致病基因。DMD基因有数千种不同突变形式,这些突变被分为两种主要类型。第一类突变是外显子缺失或重复,这类突变约占所有DMD基因突变的70%-80%。MLPA是临床检测DMD基因外显子缺失和重复的最主要方法,这也是DMD基因突变的首选诊断技术。第二类突变是点突变,包括单碱基置换、多个碱基的插入和缺失,这类突变约占20%。桑格测序和高通量测序技术是诊断DMD基因点突变的可用手段。目前,通过MLPA和测序技术的联合,大约98%左右的DMD和BMD患者都可以获得明确的基因突变诊断。对于有进行性肌营养不良家族史的孕妇,可以通过对先证者和孕妇进行DMD基因突变分析判断孕妇的携带者状态。对DMD基因突变携带者可以实现准确的进行性肌营养不良产前诊断。
什么是进行性肌营养不良
必须首先指出的是,用进行性肌营养不良来称呼我这里要说的疾病并不是非常准确的。严格来说,进行性肌营养不良是指一组由肌膜结构异常、肌肉破坏所导致的疾病,包括数十种不同的类型。我们这里所说的进行性肌营养不良其实只是指其中最常见的两种,也就是Duchenne(读音:杜欣)型肌营养不良和Becker(读音:贝克)型肌营养不良,它们也被称为杜氏肌营养不良或者贝克(贝氏)肌营养不良。由于这两种肌营养不良在疾病早期通常伴随明显的小腿肥大,所以另一个经常用于称呼这两种疾病的名称是“假肥大型肌营养不良”。
杜氏型肌营养不良的英文名称是Duchenn Muscular Dystrophy,而贝克型肌营养不良的英文名称是Becker Muscular Dystrophy,分别取英文名称的第一个字母就组成了DMD和BMD这两个缩写,这也是许多人所熟悉的疾病名称。我想强调的是,虽然我在这里根据约定俗成的习惯用进行性肌营养不良来直接指代DMD和BMD,但是确实还有许多其他类型的肌营养不良不论从发病机制还是临床表现上都与这两种疾病存在显著差异,其中相对多见的是肢带型肌营养不良、面肩肱型肌营养不良等。
进行性肌营养不良是临床常见的一种以运动障碍和肌肉萎缩为主要特征的疾病。无论是DMD还是BMD,它们致病原因都在于一种叫做“抗肌营养不良蛋白(dystrophin)”物质的功能缺陷。dystrophin蛋白是一种沟通肌细胞内外的重要蛋白,这种蛋白功能缺陷通过一系列复杂的病理过程,最终导致肌细胞死亡,在临床上即表现为以肌肉无力、萎缩为主要特征的疾病。简单来说,肌肉表面覆盖了一层膜,dystrophin蛋白是这层膜(叫做肌膜)的重要组成部分,dystrophin蛋白缺陷好像这层膜上破了一个又一个小孔,使得里面的肌肉不能得到肌膜的保护而发生破碎,最终导致进行性肌营养不良的发生。 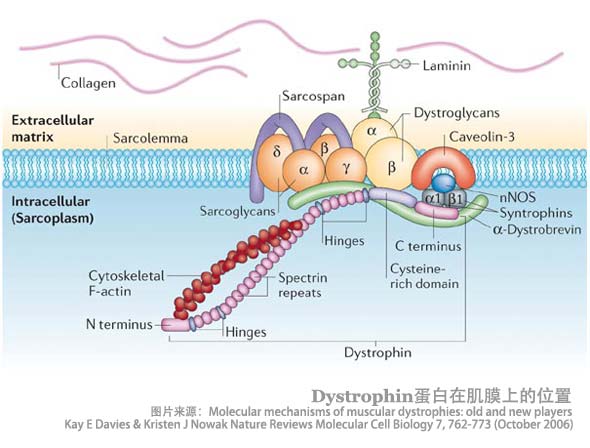
编码dystrophin蛋白的DMD基因突变是造成进行性肌营养不良发生的根本原因。DMD基因位于人类X染色体上。由于女性的性染色体为XX,而男性为XY,因此女性存在两个DMD等位基因,而男性则只有一个DMD基因。DMD基因突变遵循隐性遗传的模式。也就是说,对于女性来说,如果一个DMD基因突变,只要另一个DMD基因完整,她就不会表现出症状。而对男性来说,因为只有一个DMD基因,一旦突变就会发病。所以,进行性肌营养不良是一种典型的X连锁隐性遗传病,患者主要为男性,而女性则为携带者。据统计,男性人群中DMD患者的比例大约为1/3500,而女性携带者约为1/2300。对于单基因遗传病来说,这是一个很高的发病比率。
概括起来,进行性肌营养不良是一种由DMD基因缺陷所导致的X连锁隐性遗传病,在组织层面上造成造成肌肉结构破坏,在临床上则表现为运动能力的损害。
进行性肌营养不良的临床表现和分型
进行性肌营养不良以渐进性的运动能力损害为主要临床表现。杜氏型肌营养不良(DMD)和贝克型肌营养不良(BMD)患者在临床表现上存在相似性,因为他们都表现为运动能力的损害,也有些相同的特征性体征,如都有双侧腓肠肌的假性肥大。但是,在疾病的严重程度上,DMD和BMD患者则存在明显的差异。DMD是相对较重的类型,而BMD是相对较轻的类型。
尽管进行性肌营养不良患者事实上在运动发育方面在很小的年龄就经常会有一些落后,但是这些落后通常会被家长忽略。一般而言,走路不稳、步态异常、易摔倒等情况是进行性肌营养不良患者最初变现出的临床症状。对于DMD患者,这些情况通常发生在2-6岁之间;而对BMD患者,起病年龄的变异程度较大,可以在2-15岁之间。进行性肌营养不良患者的走路不稳是由于其近端肌无力、尤其是肢带肌无力造成的,因此这时候患者常常已经有双肩关节松弛等临床体征。由于下肢肢带肌无力,为了保持身体平衡,进行性肌营养不良患儿走路常常会挺腰凸肚,双腿慢慢向两侧迈开,表现出“鸭步”的步态特点。
双侧腓肠肌假肥大是进行性肌营养不良患者的重要特征之一。在发现走路不稳的情况以后,进行性肌营养不良患者小腿后侧的腓肠肌会显得很肥大,乍一看好像肌肉很发达一样。但是,这种肥大并不是真的肌肉发达,而是由于肌细胞变性、坏死造成的病理性肥大,因此称为假肥大。在临床上,腓肠肌假肥大是判断进行性肌营养不良的重要依据之一,典型的腓肠肌假肥大患儿家属也会自觉地发现。
在腓肠肌假肥大的同时,患者的大腿肌肉和上臂肌肉往往已经伴随一定程度的萎缩。由于大腿肌肉无力,进行性肌营养不良患儿完成一些动作会很困难,尤其表现在从仰卧位站起困难。这时候患儿必须调整到俯卧位,屈膝屈髋,双手先支撑床面,然后撑着自己的膝盖缓慢站起。这套具有特征性的动作被临床医生称为Gower's征。 Gower's征是进行性肌营养不良患者的另一个常见特征,但是并不是所有表现Gower's征的儿童都是进行性肌营养不良患者。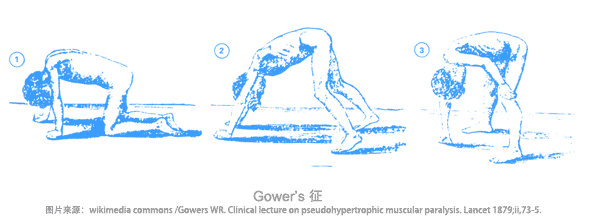
此后,随着年龄增长,进行性肌营养不良患者的运动障碍会越来越严重,活动越来越困难。总体上,进行性肌营养不良患者的肌无力从近端开始向远端发展(从上臂向前臂,从大腿向小腿),从下肢开始向上肢发展。随着受影响肌肉范围的增大和影响程度的增加,进行性肌营养不良患者会逐渐丧失运动能力。DMD患者通常在8岁左右将无法上楼梯,假肥大的腓肠肌也会随着年龄增大与其他肌肉一样逐渐萎缩。随着活动的减少,各个肢体关节也将逐步挛缩,大多数DMD患者在12岁左右都将只能依靠轮椅来活动。尽管BMD的进展方式和DMD类似,但是其进展速度要比DMD慢很多,很多BMD患者在40岁时还能够独自下地活动。
除了骨骼肌受损以外,进行性肌营养不良患者的心肌也会受到损害。90%的进行性肌营养不良患者的心功能随着疾病进展会受到影响,主要表现为肥厚性和扩张性心肌病。心力衰竭是20%DMD患者是死亡原因,而在BMD患者中死于心力衰竭的比例则达到50%。
虽然DMD和BMD的发病原因相同,也都被称为进行性肌营养不良,但是DMD患者和BMD患者的存活年限却有明显的差别。DMD患者的平均寿命在20岁左右,主要死亡原因是全身肌力下降以及呼吸肌受损造成的呼吸衰竭和肺部感染。BMD患者如果能够坚持合适的运动锻炼、加强护理、控制心力衰竭等问题,部分患者可以获得近似正常人群的预期寿命。
DMD与BMD的辅助分型
临床症状的严重程度是区分DMD和BMD的最主要依据。除此以外,基因检测和肌肉活检对于分型也有一定作用。通过外显子阅读框法则能够根据基因突变的类型来对疾病的严重程度进行预测,预测的准确性在DMD基因外显子缺失患者中相对较高。而在肌肉活检中,根据dystropin蛋白表达的下降程度以及蛋白不同结构域表达的差异也能对BMD和DMD进行分型。
在小年龄患者中,尤其在偶然发现CK、ALT等酶学指标增高而临床并无表现的患儿中,基因检测与肌肉活检对分型的预测客观上能够为疾病预后提供参考。毕竟,DMD与BMD在严重程度上差别悬殊。但是,需要注意的是,无论基因检测还是肌肉活检,对于DMD和BMD的分型判断都是辅助性质的。尽管它们的准确性相对较高,然而最终的分型依然要以实际的临床病情发展为准。
进行性肌营养不良的临床诊断
进行性肌营养不良(DMD/BMD)是临床症状相对典型的疾病,很多患者通过简单的检查可以获得相对确切的临床诊断。诊断进行性肌营养不良的重要依据包括以下几项。
- 典型的临床表现,起病时间和发病过程可以作为区分DMD和BMD的主要参考;
- 肌源性损害体征,如肌张力降低、腱反射消失等;
- 肌力下降下肢重于上肢、近端重于远端;
- 疾病过程中经历明显的腓肠肌假性肥大;
- Gower's征阳性;
- 一般不伴有上运动神经元损害体征,如病理征等;
- 不伴有智力发育落后或伴随轻度智力发育落后;
- 肌酶明显升高,CK值一般在数千甚至数万;
- 肌电图呈现肌源性损害;
- 肌肉活检呈现典型的肌源性损害改变,dystrophin蛋白表达明显下降或不表达。
有经验的医生根据临床表现和体征诊断典型的进行性肌营养不良还是较有把握的。但是,由于不同类型的肌营养不良在症状上存在很多交叉,一些肌营养不良一样可以表现出Gower's征、腓肠肌假肥大,甚至CK也能达到上万。因此,DMD和BMD的最终确诊要依赖于DMD基因检测或者肌肉活检后的dystrophin蛋白免疫组化分析。
肌酶升高与进行性肌营养不良
肌酶显著升高是诊断进行性肌营养不良的重要依据。肌酶检测简单快捷,只需要验一次血即可,一般一天就能获得结果。所谓肌酶是一些在肌肉中存在的酶,常用的肌酶包括肌酸激酶(CK)、丙氨酸氨基转移酶(ALT)、门冬氨酸氨基转移酶(AST)、乳酸脱氢酶(LDH)等。进行性肌营养不良患者肌膜被破坏,这些肌肉中的酶大量释放到血液中,造成血液中这些酶的含量升高。因此,各种肌酶升高实际所提示的是肌肉的破坏。在这些指标中,最具有代表性的是肌酸激酶CK。典型的进行性肌营养不良患者血液中的CK值常常高于参考值数十倍,达到1-2万U/ml,而正常人通常只有100-200U/ml。
尽管CK是判断进行性肌营养不良的重要依据,但是与任何疾病一样,不能依靠一项血液生化指标来做诊断。进行性肌营养不良并不是造成CK急剧升高的唯一原因,其他类型的进行性肌营养不良、横纹肌溶解症等也可能造成CK很高。同时,CK轻度升高的患者不能盲目诊断进行性肌营养不良,尤其是CK只是正常值的几倍的情况,往往提示先天性肌病等其他肌肉疾病存在的可能。对于进行性肌营养不良患者自身,CK的值也会有波动,并会随着疾病的进展缓慢下降,这种下降并不是疾病在好转,而是提示残留的肌肉组织越来越少。 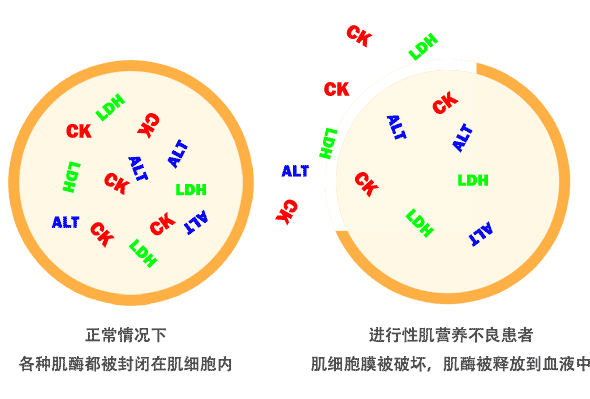
此外,还有一点必须注意。这些肌酶并不单纯在肌肉中存在,如ALT和AST在肝细胞中也大量存在,肝炎患者的ALT和AST也会升高。有些孩子在日常体检中(如入园或入学体检、因感冒腹泻等在医院验血)发现ALT和AST升高被当做肝炎反复治疗而不见指标下降,其实是进行性肌营养不良患者,这种情况并非个例。由于ALT和AST通常被作为“肝功能”检查,一旦发现问题就以为是肝有问题,因此诊断必须结合临床和其他检查综合判断。
进行性肌营养不良的肌肉活检
在DMD基因检测成为现实以前,肌肉活检一直是进行性肌营养不良诊断的金标准。由于基因检测和肌肉活检同样是进行性肌营养不良诊断的可靠方法,有了基因检测以后,很多人不愿意接受肌肉活检。其实,肌肉活检依然在进行性肌营养不良的诊断中扮演重要角色。肌肉活检可以通过免疫组化实际看到肌膜上dystrophin蛋白的表达情况,依然是对进行性肌营养不良极为准确的诊断方法。当然,肌肉活检是一种创伤性的检测,因此一般建议所有疑诊进行性肌营养不良的患者首先接受DMD基因检测,而把肌肉活检作为一种解决疑难问题的二线检测方法。在临床工作中,经常会碰到一些单纯依靠基因检测无法解决问题的现实情况,例如临床表现不典型的DMD/BMD,或者需要短时间精确确诊的患者。在这些时候,肌肉活检是一种非常可靠的诊断与排除诊断方法。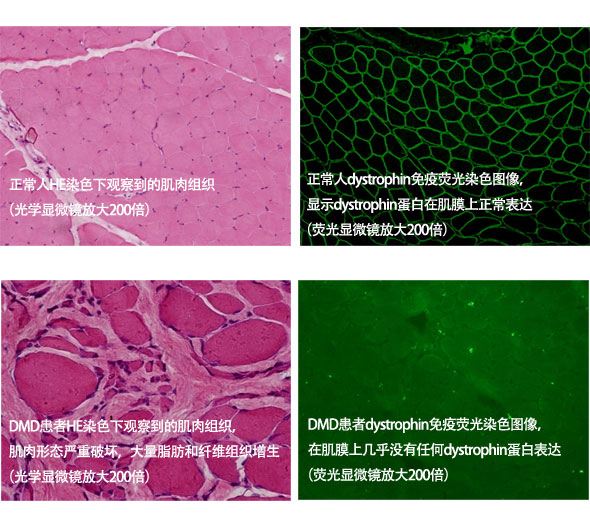
必须注意的是,要通过肌肉活检确诊进行性肌营养不良就必须使用dystrophin蛋白抗体进行免疫组化检测。常规的HE染色体或者ATPase等染色虽然对疾病判断有一定作用,然而不是确诊的标准。在上图中,你可以很清楚看到dystrophin蛋白在正常人和DMD患者肌膜上表达的巨大差异。由于大多数人不会因为同一种疾病接受两次肌肉活检,因此在接受肌肉活检前应确切了解活检项目是否包括针对dystrophin蛋白的直接检测。而对提供活检的单位,也应该为DMD/BMD患者准备相应的抗体,以体现肌肉活检出价值。
(本文中的肌肉活检图片由复旦大学附属儿科医院李西华主任提供。)
DMD患者的治疗原则
进行性肌营养不良,无论是杜氏型肌营养不良(DMD)还是贝克型肌营养不良(BMD),在当前都是无法治愈的疾病,因此都不可能通过药物、手术来完全改变病情的进展。由于临床表现上的相似性,这DMD和BMD在治疗上也有相似的原则,即治疗都是以提高生活质量为主要目标,而不是以治愈疾病为目标。由此,合适的康复锻炼和对症处理并发症是疾病治疗的核心内容。但是,DMD和BMD在预后上存在很大的差异,因此在实际处理过程中需要区别对待。
DMD患者的病情发展一般经过包括以下几个过程:幼儿期没有明显症状或者有走路较慢、不稳、易摔倒等不明显的表现;大约在3-6岁左右患儿走路不稳、跑不快的表现会逐渐明显;10-12岁以前,运动能力进一步下降,无法上楼以至于走路困难;大多数DMD患者在12岁左右丧失走路的能力;运动能力损害逐渐累积更多肌肉,全身肌肉萎缩,预期寿命一般在20岁左右。
虽然不是一个容易接受的事实,但是目前并没有有效的方法来改变这一疾病过程。治疗的目的是尽可能延缓肌肉萎缩的过程,相对提高运动能力,改善患儿的生存质量。必须强调,改善生活质量是DMD治疗的核心内容。 因此,对于DMD孩子的处理,应该综合评估治疗手段的利弊以及治疗与生活的平衡,而不应该因为治疗而反而影响了孩子的正常生活。
具体来说,小年龄段的孩子、临床症状不明显的孩子不需要接受任何治疗,他们应该和正常孩子一样生活,享受快乐的时光。当孩子的运动能力受到明显的影响,应当及时地寻求运动康复。对症的运动康复能够让孩子发挥现有的运动潜能,良好的姿势有助于更好地活动,同时能够避免肌肉的快速萎缩和关节的挛缩。DMD患儿的康复以居家康复为主,即在康复医生的指导下在家中完成康复,定期到医院随访即可。运动康复是一个专业而复杂的学科,简单来说,原则是要促进主动运动,无法主动运动的部位要辅以被动运动,要保持全关节范围的运动以避免僵硬和固定。找到一个有经验的康复医生指导康复是很重要的。
在康复以外,随着疾病的进展,DMD患儿可能发生一些其他的医学问题。比如,肌力下降导致容易发生坠积性肺炎,加强护理、保持良好的居住环境就显得很重要。有些患者会发生脊柱侧弯,合适的支具能够起到支撑和固定的作用,缓解脊柱弯曲对内脏的压迫。这些特殊的并发症既需要专科医生来处理,更需要家长和家人的帮助。
在营养方面,DMD患者应该补充足够的蛋白质,但是要控制体重。体重增加会显著影响运动能力。因此在蛋白质的选择上要多采用脂肪含量低、吸收好的优质蛋白质,比如鱼肉、禽类等。使用BMI指数衡量指数是相对科学的方法。
DMD患儿的心肌同样可能受到损害,心功能下降不但是造成患儿死亡的原因,也严重影响运动能力。幸运的是,心肌损害可以通过一些药物得到有效的控制。因此,建议DMD患者定期做心电图和心脏彩超检查,通常一年一次为宜。如果发现心功能下降,可以及时使用相应的药物来控制症状。
DMD患者的激素治疗
长期激素治疗是延缓DMD患者病情进展的有效方法,具有相应的循证医学证据。激素治疗的目的是缓解症状,增加患儿的活动范围,改善生活质量。激素治疗无法改变DMD的疾病过程,这一点是必须注意的。合理使用激素能够对部分DMD患儿是有益的,但是激素治疗存在许多潜在风险,在使用激素前应该综合评估治疗的利弊再以定夺。
激素治疗的副作用主要包括免疫功能下降导致容易感染、精神和行为改变、骨质疏松、糖耐量下降、消化系统溃疡、体重增加、白内障等。这些副作用既与激素剂量有关,也与个体差异相关。总体来说,服用时间越长,发生副作用的风险就越高。此外,激素治疗需要坚持正规服用,不能随意停药减药。因此,是否使用激素治疗很大程度上取决于家长的态度。如果无法坚持规范给药,无法定期到医院随访,那可能还是不要使用为妥。
激素治疗的另一个问题是追求短期效果而大剂量使用激素。大剂量激素治疗能够迅速改善患者的运动能力,但是这种改善往往是短暂的。大剂量激素的副作用很多,有时候可以在短时间内造成体重急剧增加,从而使患者的运动能力下降更快。
正规的激素治疗是一种长期使用小剂量激素的方法。欧美国家的指南推荐伎俩是0.5-1mg/kg·d强的松。有每日给药的方案,也有不同的间歇给药方案。使用哪种方案既取决于治疗效果,也决定于医生的习惯。国内目前尚没有确切的询证医学证据指导DMD的激素治疗。由于西方人在激素的耐受性方面明显好于中国人,所以作为患者家长不能只盯着西方国家的指南,而应该听从医生的建议。
激素的起始治疗时间也并没有统一的认识。一般建议在运动发育达到高峰期的时候服药,也就是说在运动功能下降之前开始服药。也有人建议从诊断就开始用药。但是,达成共识的意见是,如果孩子的运动能力已经明显受损,例如上楼已经很困难,这时候再使用激素往往效果不佳。对于使用激素的患者必须正规服用,并且定期随访。使用激素同时应注意补钙、控制体重、忌食过度刺激肠胃的食物、注意预防感染,如果有不良反应,应该及时到医院就诊。
DMD患者的中医和针灸治疗
总体来说,没有任何证据证明中医能够治疗DMD。中医是一种有效并且博大的医学体系,但是不能把中医当做治疗西医无法治好疾病的解决方法,这种思路是错误的,而很多患者家属都抱有类似的认识。单纯的中医治疗虽然无效但是也不见得有害。然而,目前有些单位打着中药的幌子,却在中药中添加不标明含量的激素甚至是大剂量激素,服用这样的“中药”就会很有问题。当然,这并不是中医本身的问题,但是确实需要注意这些问题的客观存在。
就运动能力的改善来说,针灸可能是一个可以尝试的方法。我并不了解针灸,但是针灸在神经肌肉疾病的症状缓解方面有时候确实有神奇的效果。作为一种改善症状的手段,如果针灸确实对孩子有效,同时又不是那么痛苦,那么这是一种可选的方法——其实激素治疗的目的不也是一样的吗?
基因治疗与干细胞治疗研究
关于DMD的基因治疗研究是相关领域的一个热点课题,不同的课题组采用不同的方法在这一领域做着工作。目前,外显子跳跃是相关方法中研究较多的一种。针对51号外显子跳跃的治疗虽然获得了FDA的批准,但是疗效尚存争议。外显子跳跃的原理是通过RNA干扰人为剪去一个或者多个外显子,其目的是恢复DMD基因的阅读框,部分恢复蛋白功能,实现将DMD患者转变为BMD患者从而控制症状的效果。
干细胞治疗也是近年治疗研究的前沿。与基因治疗一样,干细胞治疗目前主要用于研究,尚无法在临床开展治疗。无论是基因治疗还是干细胞治疗,它们都是未来治疗的希望。可是,当前并没有任何临床治疗成功的报道。对于这个事实患者家属应该充分认识。家长的求治心切是可以理解的。在了解真相、知情同意的原则下,参与任何有成功可能的临床试验无可厚非。但是,如果医疗机构以收费治疗的形式提供任何所谓的干细胞治疗和基因治疗,那么就要提高警惕,避免不必要的精力和物力损失。
BMD患者的治疗原则
与DMD不同,大多数BMD患者都可以存活很长时间,一些患者能够获得接近于正常人的预期寿命。因此,BMD的治疗是一个贯穿一生的漫长过程。BMD患儿发病年龄较晚,有很多患者要到上小学甚至上中学时才逐渐表现出症状。与DMD一样,在患儿没有表现出明显运动问题的时候,不需要任何治疗,而应该让孩子和正常人一样去生活去学习。激素治疗对BMD是无效并且有害的,BMD患者不应接受激素治疗。
与DMD一样,当运动能力发生问题以后,康复锻炼是最佳的手段。由于BMD患者生存年限长,发病缓慢,康复锻炼可以起到更好的效果。良好的康复锻炼可以大大改善BMD的发病过程,增加患者自主活动的范围和时间,明显提升生活质量。
不同于DMD,影响BMD患者生命的首要因素是心肌损害。因此,BMD患者应该将心肌功能作为主要管理目标。BMD患者应该定期进行心脏方面的检查,一般建议每年做一次心脏彩超和心电图,及早发现问题及早治疗。通过合适的治疗能够极大程度降低心力衰竭的发生可能,并且保持较好的心功能。良好的心脏功能不但有助于BMD患者更好的活动,也能够大大提高BMD患者的存活年限。
总体来说,对BMD患者更为强调的不是疾病治疗或者什么新技术的研发,而是长期的健康管理。如果所有慢性病一样,患者如果能够学会管理疾病,BMD确实是一种相对可控的遗传疾病。
DMD基因检测
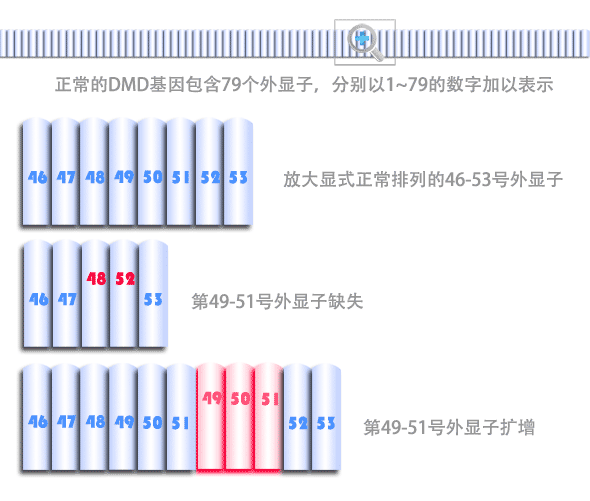
DMD基因突变是已知导致进行性肌营养不良(包括DMD与BMD)发生的唯一原因。DMD基因突变检测是诊断进行性肌营养不良的可靠方法。DMD基因是人类基因组中最大的基因,总共包含79个外显子(你可以理解为由79段组成),每一个外显子发生问题都会导致进行性肌营养不良的发生。DMD基因突变形式据统计达到四、五千种之多,这使得临床检测DMD基因突变有一定的困难,这制约了以往DMD基因突变检测的开展。近两年,随着分子诊断技术的进步,DMD基因突变的临床检测获得了长足的发展。
总体来说,DMD基因的突变可以分为两大类:第一类是涉及到整个外显子的缺失或重复,第二类是外显子内部单个或者几个碱基的突变。举个例子,把DMD基因比做一套书,这套书由79本组成。第一类突变是书的本数发生了变化,外显子缺失就好比是丢了一本或者几本书,外显子扩增就好似多了一本或者几本书。而第二类突变是指书的本数没有改变,还是79本,但是某本书里面少了一页,或者有一页印刷错误。
这两种基因突变类型对应不同检测方法,这在一定程度上增加了DMD基因检测的复杂性。
DMD基因外显子缺失/重复检测
在DMD基因突变类型中,单个或多个外显子缺失约占60%~70%,单个或多个外显子扩增约占10%。因此,DMD基因突变有70%~80%是由外显子缺失或者重复造成的。外显子缺失和重复的检测相对简单,而且检出率高,因此这已经成为了目前进行性肌营养不良的首选诊断方法。对于临床诊断或者疑诊为DMD和BMD的患者,一般首先会考虑检测DMD基因外显子缺失或重复。目前常用的检测方法有以下几种:
- 多重PCR:多重PCR(Multiplex PCR)是最传统的DMD基因外显子缺失检测方法。它只能检测热点外显子,并且只能检测缺失而不能检测重复。同时,多重PCR体系优化复杂,PCR反应之间相互影响,容易发生假阳性。目前,在有MLPA条件的实验室,应该采用MLPA替代多重PCR。
- MLPA:MLPA是当前针对DMD基因外显子缺失和重复的标准检测技术。MLPA可以通过两个反应覆盖DMD基因全部79个外显子。它的缺点是操作相对复杂,对质控要求较高。此外,MLPA的单外显子异常结果和可疑结果需要通过其他方法进一步验证。
- 高通量测序:高通量测序不但可以检测DMD基因外显子缺失和重复,还能检测点突变。现阶段,高通量测序对外显子缺失与重复的判断(尤其是重复)要差于MLPA,同时高通量测序价格昂贵。
在现有技术条件下, MLPA应是针对DMD外显子缺失和重复的首选检测方法,也是临床诊断进行性肌营养不良的首选基因检测方法。
DMD基因点突变检测
通常意义上所说的点突变包括单碱基突变和多个碱基的插入或缺失,这类突变在DMD突变中约占20%。目前,可用于DMD基因点突变检测的方法主要有两种:
- 桑格测序:桑格测序是传统的测序技术。通过PCR反应将DMD基因的79个外显子一一扩增出来然后进行测序能够准确检测出DMD基因的点突变。桑格测序的缺点是费时费力,做一个患者检测就需要至少79个反应,成本也不低。综合考虑成本效益,这愿意开展该检测的实验室非常少。
- 高通量测序:高通量测序技术大大简化了DMD基因点突变检测的过程,是目前DMD基因点突变检测的标准方法。在有条件的情况下,结合MLPA和高通量测序,将大大提高DMD基因突变检出率,并且简化临床流程。
无论采用哪种方法进行DMD基因点突变检测,基因型表型关联都是点突变检测中的主要问题。由于人类基因组上存在大量不同于标准序列的正常碱基变异, 测序是以标准序列为基准进行比对的。测序所获得的突变结果是否真的与疾病有关是一个相当复杂的问题。因此,基因测序结果需要由了解基因型表型关联的专业医生进行解读。在实践中,确实有一些基因突变的致病性是根据现有积累无法明确的。
DMD基因检测流程
结合现有的基因检测手段,大约98%的进行性肌营养不良患者都能够获得确切的基因诊断。剩余2%患者突变未能检出有多种原因。可能是基因突变位于内含子或者启动子区,这些区域目前是无法在临床开展检测的;也可能是检测过程的错误漏掉了基因突变,基于测序技术的原理,这种漏检的几率是客观存在的。
由于外显子缺失和重复是最常见的DMD基因突变形式,因此一般建议患者首先接受MLPA检测。对MLPA检测阴性的患者需要进一步进行临床评估。如果临床是典型的DMD或者BMD,则可以直接做点突变检测;如果临床不典型,建议先通过肌肉活检等手段确定诊断再进行点突变检测。对于两步检测(第一步:缺失重复、第二步:点突变)都正常但是没有确诊的患者,应该在基因检测后通过肌肉活检最终确诊或者排除诊断。
进行性肌营养不良的预防
DMD基因突变是已知导致进行性肌营养不良的唯一原因,因此在怀孕期间通过对胎儿进行DMD基因突变检测能够有效预防进行性肌营养不良的发生。目前,通过各种检测手段,DMD基因突变的检出率可以达到约98%的水平,所以大多数进行性肌营养不良都是可以预防的,并且在临床应用方面并不复杂。关键是需要踩好步点,不要错过合适的检测时机
预防进行性肌营养不良再发
对于曾经生育过进行性肌营养不良患儿的父母,在再次怀孕以后,只需在怀孕中期(通常在16-20周)进行一次羊膜腔穿刺,抽出少量羊水后进行DMD基因突变检测,即可完成产前诊断。这看起来是一个简单的过程,但是有很多需要注意的方面。
首先,产前诊断必须遵循一般的先证者-携带者-产前诊断的三部曲流程。家长要做的第一件事情是带孩子到医院确诊疾病,并且找到基因突变。这一点对进行性肌营养不良的产前诊断来说尤为重要。DMD基因突变形式复杂,尤其是点突变患者往往要经过两步检测才能被检出。这个检测过程在不同单位所需时间不同,而且基因检测也常常容易碰到一些事先难以预料的问题。理想情况下家长应该要在怀孕前做完先证者的诊断。在明确了孩子的基因突变之后,确认孕妇的携带者情况与后续的产前诊断就很容易了。但是,如果先证者之前没有明确DMD基因突变,孕妇在16-20周的时候直接要求做产前诊断就显得很麻烦。所以,必须记住,一定要在怀孕前明确孩子的基因突变,做好准备,才能让产前诊断变得顺利。
其次,进行性肌营养不良的产前诊断针对的是DMD基因,做染色体是没用的。所以,一定要做针对DMD基因的羊水检测,而不能单纯做羊水染色体检查。由于DMD是一种X连锁隐性遗传病,因此羊水染色体在判断胎儿性别上有协同作用。
再者,对于基因突变未检测出DMD突变的进行性肌营养不良患者,可以通过STR连锁分析的方法辅助进行产前诊断。但是,STR连锁分析有两个条件。第一,先证者的进行性肌营养不良诊断必须明确,最好有肌肉活检dystrophin蛋白组化证据;第二,有家族史的患者更为适用。
最后,有一部分进行性肌营养不良患者是新发突变,即孩子检出DMD基因突变而母亲并没有检出突变。对于这种情况,母亲再生进行性肌营养不良患儿的可能性非常低。不过因为存在生殖细胞嵌合的情况,依然建议在怀孕后进行DMD基因产前诊断以防万一。
进行性肌营养不良产前诊断的大致流程如下图所示:
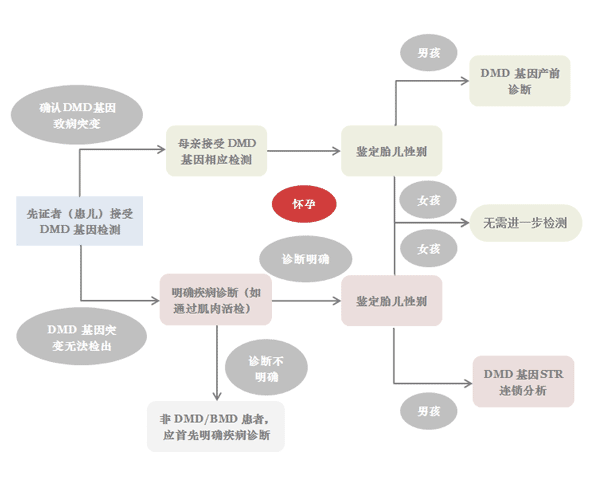
家族中有进行性肌营养不良患者的情况
进行性肌营养不良是一种发病率比较高的疾病,而且症状比较容易识别,临床诊断率相对较高。因此,如果在家族中有人患上进行性肌营养不良,通常很容易被家族里的其他人所关注。当有亲缘关系的女性考虑生孩子时,她们也经常会想到这一情况,希望知道自己生孩子是不是有风险,如果有风险的话有没有办法来避免。
进行性肌营养不良是一种X连锁隐性遗传病,所以首先要判断家族中的患者是否可能对你的生育有影响。比如说,如果你的姑姑(父亲的姊妹)生了一个进行性肌营养不良的患者,那么你完全不必因此担心,因为根据X连锁隐性遗传的规律,你不可能携带这个异常的DMD等位基因。通常,以下是女性可能携带致病DMD等位基因的一些常见情况。
- 亲兄弟是进行性肌营养不良的患者;
- 舅舅是进行性肌营养不良的患者;
- 姨表兄弟(母亲姊妹的儿子)是进行性肌营养不良的患者。
如果是上面这些情况,那么你可能是DMD基因突变携带者,也可能完全正常。因此,首先需要解决的问题不是肚子里的孩子究竟会不会是进行性肌营养不良患者,而是你本人是否是DMD基因突变携带者。对于这样的情况,最佳解决路径是让家族里的先证者,也就是那个患病的亲戚接受DMD基因检测,然后再判断你的携带状态。所以,这件事情也有三步。第一步是家族中的先证者明确诊断并找到DMD基因突变,第二步是检测要怀孕的女性本人是否为携带者。如果找到先证者的基因突变,而你本人不带该基因突变,那么事情到此就结束了。如果你携带了与先证者相同的突变,那么第三步是产前诊断。下图为你展示了完整的临床处理流程。需要注意的是,这个过程需要比较长的时间,因此同样应该在备孕期间完成先证者检测,而不是到怀孕中期再寻求检测。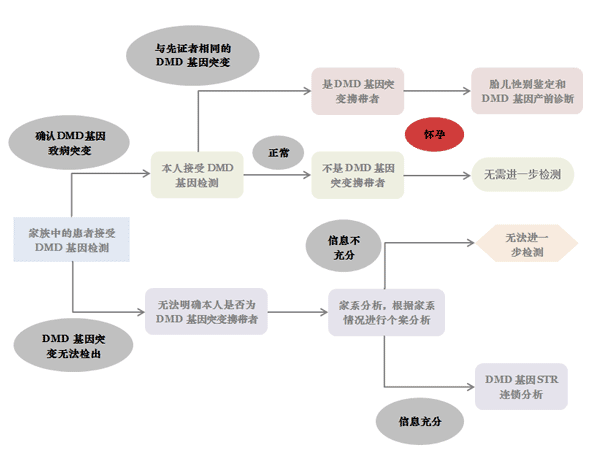
这虽然是处理类似情况的最佳选择,但是有时候这条路未必能走通,原因在于很多家庭中的先证者无法接受检测。这或者是因为先证者已经去世,或者是因为无法取得联系。当家族中的先证者或者确切的携带者无法接受检测的时候,那么唯一的方法是对准备怀孕的女性本人进行DMD基因突变检测,一般联合外显子缺失/重复和点突变两种检测方法以覆盖所有突变谱。对于明确突变的女性,进一步采取产前诊断的方法;对于无法找到突变的女性,虽然无法采取进一步产前诊断方法,但是这可以将DMD基因突变携带率降低到很低的水平。
也许有人会有疑问,既如此,为什么还要对先证者做检测?对准备怀孕的女性本人检测不是一样的吗?在测序技术被广泛应用于DMD基因突变临床检测之前,这是完全不一样的;在DMD点突变检测变得可能以后,两者之间的区别变小了。但是,先证者诊断是产前诊断的一般原则,这能够避免发生许多不能预测的事情,而且可以大幅增加检测的可靠性。因此,但凡家系中的先证者能够接受DMD基因检测的都应首先让先证者接受检测,而且时间必须要早,要在怀孕之前。
父亲是进行性肌营养不良患者的情况
有一种比较少见的情况,即父亲是进行性肌营养不良患者。贝克型肌营养不良的患者可以获得接近正常的预期寿命,娶妻生子也是很正常的事情。对于贝克型肌营养不良患者来说,生育的男孩都是健康的,不会成为进行性肌营养不良患者(很多人不理解的事实,但是这就是X连锁隐形遗传病的规律);而生育的所有女孩都是致病DMD基因携带者。因此,如果你的父亲是进行性肌营养不良患者的话,你本人一定是DMD基因突变携带者。在这种情况下,可以直接接受DMD基因检测,也可以让父亲先接受DMD基因检测。尽管两者没有明显区别,但是我还是建议现对父亲,也就是先证者进行检测。这是合理的逻辑,同时鉴于DMD基因的特点,对男性进行检测在技术上会更可靠。
参考阅读
以下是一些关于进行性肌营养不良的参考资料,主要提供了一些关于疾病与DMD基因的常用专业文献与工具,仅供专业人员参考。
- OMIM #310200:MUSCULAR DYSTROPHY, DUCHENNE TYPE; DMD
- OMIM #300376:MUSCULAR DYSTROPHY, BECKER TYPE; BMD
- OMIM *300377:DYSTROPHIN, DMD
- CCDS 14233: DMD Gene, Homo Sapiens
- DMD (ENSG00000198947) variation table from 1000 genomes
- LOVD DMD Gene mutation database
- UMD-DMD mutation database
- Leiden DMD gene reading frame checker